Hunter Sendromu (MPS II)
Hunter Sendromu (MPS II) Nedir?
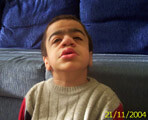
MPS, Glikozaminoglikanları (GAG) yıkan enzimlerden birinin eksikliğinin lizozomlarda GAG birikmesine yol açtığı bir Lizozomal Depo Hastalığı (LSD) türüdür.1
Bu hastalıklar tipik olarak çocuklukta alt tipe bağlı olarak çeşitli semptomlarla ortaya çıkar ve birçok organ sistemini etkileyebilir.1 Hangi enzimin eksik olduğuna bağlı olarak MPS bozukluklarının farklı tipleri vardır. MPS I (Hurler, Hurler–Scheie, Scheie Sendromu), MPS II (Hunter Sendromu), MPS III (Sanfilippo A, B, C, D Sendromu), MPS IV (Morquio A, B Sendromu), MPS VI (Maroteaux–Lamy Sendromu), MPS VII (Sly Sendromu), MPS IX (Natowicz Sendromu) gibi farklı tiplerde belirtiler, hastalığın şiddeti ve ilerleme hızına göre değişkenlik gösterir. Bununla birlikte, boy kısalığı, bilişsel bozukluk, iskelet bozuklukları, kaba yüz özellikleri, işitme kaybı, kalp-damar hastalıkları gibi bazı klinik özellikler yapı olarak MPS tiplerinde benzerdir.2
Hunter sendromu (MPS II) birkaç lizozomal depo hastalığından (LSD) biridir. LSD’ ler, hücrelerin belirli molekülleri düzgün bir şekilde parçalayamadığı durumlardır. Hunter sendromunda, iduronat-2-sülfataz (I2S) denilen bir enzim eksiktir veya bazen tamamen yoktur.2
Sağlıklı bir hücrede, I2S, glikozaminoglikanlar (GAG’ lar) olarak bilinen belirli molekülleri parçalar. Bu moleküllere daha önceden mukopolisakkaritler denildiğinden, Hunter sendromu, mukopolisakkaridoz tip II (MPS II) olarak da bilinir.3
Eğer I2S eksikse veya yoksa, hücrelerin düzgün çalışmasını önleyen GAG’ lar oluşur. Tüm sağlıklı hücreler (kırmızı kan hücreleri hariç) I2S enzimini üretir, bu nedenle eksikliği vücudun herhangi bir bölümünü etkileyebilir. Bu nedenle Hunter sendromunun çeşitli organlarda semptomları olabilir. 1
Belirti ve Bulgular
Hunter sendromunun çeşitli belirti ve bulguları vardır. Hunter sendromu (MPS II) vücudun herhangi bir bölümünü etkileyebilir. Hunter sendromunun bulguları, bunların ilerlemesi ve şiddeti her insanda farklıdır.4
Bu belirti ve bulguların birçoğunun çocuklukta yaygın olduğunu ve bunların bir birleşiminin Hunter sendromunun işaretçisi olabileceğini unutmamak gerekir. Hastaların hepsinde tüm belirti ve bulgular görülmez ve hastalık farklı şekillerde ilerler, bu nedenle tipik bir hasta deneyimi yoktur.4
İki tip Hunter sendromu (MPS II) vardır; bunlar nöronopatik (bilişsel bozukluğu olan) ve nöronopatik olmayan (bilişsel bozukluğu olmayan) olarak bilinir.5
Her iki tipte de vücudu etkileyen belirti ve bulgular görülür, ancak nöronopatik tipte beyni ve sinir sistemini etkileyen semptomlar da görülür ve bu da davranış ve gelişimin de etkilendiği anlamına gelir. Hunter sendromlu 10 kişiden yaklaşık 7′ sinde nöronopatik tip hastalık vardır.5
Semptomlar nöronopatik tipte genellikle 2-4 yaşları arasında görülürken, nöronopatik olmayan tip genellikle 10-12 yaşlarında semptomlar gösterir.5
Genel olarak belirtiler:
- Davranış Problemleri (Hiperaktivite, inatçılık, saldırganlık)
- Gelişimde gecikme
- Nöbetler
- Belirgin kaş, geniş burun ve kalın dudaklar gibi belirli yüz özellikleri
- Görme sorunları
- Büyük dil
- Şekli bozuk dişler
- Eklem sertliği, içe kıvrık parmaklar, Karpal Tünel sendromu
- Göbek veya kasık fıtığı
- Sık kulak enfeksiyonları, işitme kaybı, uzun süreli burun akıntısı
- Sık öksürük ve soğuk algınlığı
- Hırıltılı solunum ve horlama problemleri
- Üfürüm veya kalp kapak hastalığı4,5,6,7,8
Hunter sendromu (MPS II) kalıtım yoluyla nasıl aktarılır?
Hunter sendromu (MPS II) genetik bir hastalıktır. Hunter sendromunda, iduronat-2-sülfataz (I2S) enzimini kodlayan gende bir mutasyon (değişim) gerçekleşir; bu, enzimin düzgün çalışmasını durduran hatalarla üretildiği veya enzimin hiç üretilmediği anlamına gelir.9,10
Özetle, Hunter sendromuna neden olan gen (IDS geni), X kromozomunda yer alır, bu nedenle etkilenmiş bir kromozomu kalıtım yoluyla alan bir erkekte Hunter sendromu gelişir. Kadınlarda iki X kromozomu vardır, bu nedenle bir kadın, etkilenmiş bir kromozomu kalıtım yoluyla alırsa, olguların büyük çoğunluğunda kadında hastalık gelişmeyecektir, ancak kadın taşıyıcı olacaktır (yani mutasyona uğramış geni çocuklarına aktarabilir).9,10
Hunter Sendromu (MPS-II) Tanısı ve Testleri
Hücrelerde biriken GAG’ ların bazıları vücuttan idrarla atılır, bu nedenle idrardaki GAG düzeyinin aşırı derecede yüksek olması bir MPS hastalığına işaret edebilir. İdrardaki GAG düzeylerinin testi genellikle MPS hastalığından şüphelenilmesi durumunda yapılan ilk testtir. İdrar testleri invaziv değildir (idrar örneğinin test edilmesini gerektirir) ve yaygın olarak yapılır.1 İdrardaki GAG düzeyleri sadece Hunter sendromunda (MPS II) değil, diğer MPS hastalıklarında da artar; bu nedenle Hunter sendromunu doğrulamak veya ekarte etmek için başka testler gerekebilir.4
İdrardaki GAG düzeyi aşırı derecede yüksekse veya ailede MPS II öyküsü varsa, iduronat-2-sülfataz (I2S) enziminin aktivitesi kan örneği kullanılarak test edilebilir. İkinci bir sülfataz enziminin test edilmesi, farklı bir hastalık olarak, tüm sülfataz enzimlerinin etkilendiği bir lizozomal depo hastalığı (LSD) olan çoklu sülfataz eksikliği olasılığını ortadan kaldıracaktır.4
Hunter sendromunda (IDS) mutasyona uğramış genin test edilmesi insanları taşıyıcı olarak tanımlayabilir; bu da aile planlaması hakkında bilgilendirme yapılmasına yardımcı olabilir. IDS geninin 500′ den fazla farklı mutasyonu gözlemlenmiştir ve bu değişkenlik hastalık semptomlarının tahmin edilmesini zorlaştırmaktadır. Bununla birlikte, IDS geninde büyük ölçekli değişikliklere (genetik materyalin delesyonları gibi) neden olan mutasyonlar ile nöronopatik Hunter sendromu (MPS II) arasında bir ilişki bulunmaktadır.13
Mutasyon tanımlandıktan sonra, hangi aile üyelerinin mutasyona uğramış gene sahip olma riski altında olabileceğini görmek için bir soy ağacı (aile ağacı) analizi yapılması tavsiye edilir. Genetik hastalığın kalıtımı ve sonuçları hakkında bilgilendirme yapılması için aile üyelerine genetik danışmanlık sunulmalıdır.12,13
Hunter sendromu (MPS II) doğumdan önce teşhis edilebilir. Bu tespit, I2S enziminin, plasenta dokusundaki veya amniyotik sıvıdaki aktivitesi ölçülerek gerçekleştirilir.14
Hunter Sendromunda (MPS-II) Tedavi
- ERT (Enzim replasman tedavisi)
Tedavide vücuda damar yoluyla eksik olan enzim enjekte edilir. MPS II, iduronat-2-sülfataz (I2S) enzim eksikliğinden kaynaklanmaktadır.15
Elaprase (İdursulfaz), altta yatan enzim eksikliğinin yerine konmasına yardımcı olan rekombinant, saflaştırılmış bir insan I2S formudur.15
MPS II hastalarının uzun dönem tedavisinde endikedir.15 Klinik çalışmalarda heterozigot kadınlar dahil edilmemiştir.
Seçilmiş somatik parametreleri düzeltmekte ve/veya stabilize etmektedir.15-16-17
Rekombinant human idursulfaz, ilk olarak 2006 yılında ABD’de onaylanmıştır ve şu anda 70 den fazla ülkede onaylanmış durumdadır.15
Önemli Not: MPS ve benzeri lizozomal hastalıklarıyla ilgili olarak sitemizde yer alan derlemeler, gönüllü hekimlerimiz tarafından, uluslararası kaynaklar referans alınarak yapılmıştır. Amacımız, hasta ve hasta yakınlarını, lizozomal depo hastalıkları hakkında bilgilendirmek ve hastalık farkındalığını arttırmaktır. Sitemizde yer alan bilgiler, her ne kadar tıbbi bilgi niteliği taşısa da sadece bilgilendirme amaçlıdır; kesinlikle tanı, tedavi veya klinik kararlar için kullanılmamalıdır!
Referanslar
- Parker H and Bigger BW. J Neurochem. 2019;148(5):639-51.
- Stapleton M, et al. Mol Genet Metab. 2018;125(1-2):4-17.
- Wraith JE, et al. Genet Med. 2008;10(7):508-516.
- Amartino H, Hunter syndrome (mucopolysaccharidosis II) – the signs and symptoms a neurologist needs to know. Eur Neurol Rev 2015; 10(01): 90-94.
- Kampmann C, et al. Prevalence and characterization of cardiac involvement in Hunter syndrome. J Pediatr 2011; 159(2): 327-331.
- Demydchuk M, et al. Insights into Hunter syndrome from the structure of iduronate-2-sulfatase. Nat Commun 2017; 8: 15786.
- Jones SA, et al. Mortality and cause of death in mucopolysaccharidosis type II—a historical review based on data from the Hunter Outcome Survey (HOS). J Inherit Metab Dis 2009; 32(4): 534-543.
- Keilmann A, et al. Hearing loss in patients with mucopolysaccharidosis II: Data from HOS – the Hunter Outcome Survey; J Inherit Metab Dis (2012) 35:343–353.
- Martin R, et al. Recognition and diagnosis of mucopolysaccharidosis II (Hunter syndrome). Pediatrics 2008; 121(2): e377–e386.
- MPS Society; Guide to Understanding Mucopolysaccharidosis II (MPS II) Hunter Disease; https://www.mpssociety.org.uk/mps-ii.
- Demydchuk M, et al. Insights into Hunter syndrome from the structure of iduronate-2-sulfatase. Nat Commun 2017; 8: 15786.
- Jones SA, et al. Mortality and cause of death in mucopolysaccharidosis type II—a historical review based on data from the Hunter Outcome Survey (HOS). J Inherit Metab Dis 2009; 32(4): 534-543.
- Muenzer et al. Multidisciplinary management of Hunter syndrome. Pediatrics 2009; 124(6): e1228-e1239.
- Muenzer J. Early initiation of enzyme replacement therapy for the mucopolysaccharidoses; Molecular Genetics and Metabolism 111 (2014) 63–72.
- Elaprase® summary of product characteristics, 2016
- Muenzer, J. et al. Genet Med 2013; 15: 849
- GIUGLIANI, R. et al. Genet Med 2014; 16: 435–441.

